지난 17일 HLB 리보세라닙 FDA승인 거절로 HLB가 붙은 종목들 총 8개가 하한가를 기록했습니다.
시가총액이 HLB 그룹에서만 무려 5조 원 이상 증발했습니다.

오늘은 HLB 하한가 쇼크, 리보세라닙 FDA 승인 거절에 대해서 알아보겠습니다.
HLB 하한가 쇼크, 리보세라닙 FDA 승인 거절
지난 17일 HLB는 리보세라닙 FDA 승인 거절 소식에 하한가로 곤두박질쳤습니다.
HLB그룹주 시가 총액이 무려 5조원 증발하며 코스닥 하락을 주도했습니다.
하한가에도 매도 물량이 쌓여 있어 추가 하락이 예상되고 있습니다.

리보세라닙 FDA 승인 거절 이유
리보세라닙은 간암 표적 항암제로 글로벌 13개국에서 임상3상을 마쳤습니다.
리보세라닙은 생존 기간을 늘리는데 효과가 있다고 하며 투여 중단율도 낮다고 합니다.
HLB가 리보세라닙을 미국 FDA에 신약 허가를 요청했는데 지난 17일 거절되었습니다.
거절 이유는 리보세라닙과 같이 사용되는 면역항암제 칼렐라맘에 대한 자료가 불충분하다는 점과 임상 과정에 대한 자료가 미흡했다는 점입니다.
FDA는 이를 보충하기 위해 CRL(보완 요구 서한)을 HLB에 보냈습니다.
미 FDA 허가 도전 중인 후기 임상단계 국산신약 후보
| 품목(물질)명 | 개발사 | 적응증 | 개발단계 |
| 케이캡 | HK이노엔 | 위식도역류질환 | 하반기 임상 3상 완료 및 FDA 허가 전망 |
| 바토클리맙 | 한올바이오파마 | 중증근무력증(MG) | 하반기 임상 3상 탑라인(주요지표) 확인 예상 |
| AR1001 | 아리바이오 | 알츠하이머병 | 미국 등 11개국서 1150명 대상 임상 3상 중 |
| TG-C | 코오롱티슈진 | 무릎 골관절염 | 미국 임상 3상 진행 중, 올 상반기 투약 완료 |
HLB 전망
HLB 측은 최종 보완 요청서를 받았지만 리보세라닙 이슈가 아니며 FDA 보완 요구서안 내용이 충분히 보안 가능한 부분이라고 언급했습니다.
리보세라닙의 효능이나 부작용의 내용이 아니었기 때문에 보완 요구서안 내용을 충분히 충족시키는 과정이 생긴다면 오히려 이것은 매수 기회라는 시각도 같이 나오고 있습니다.
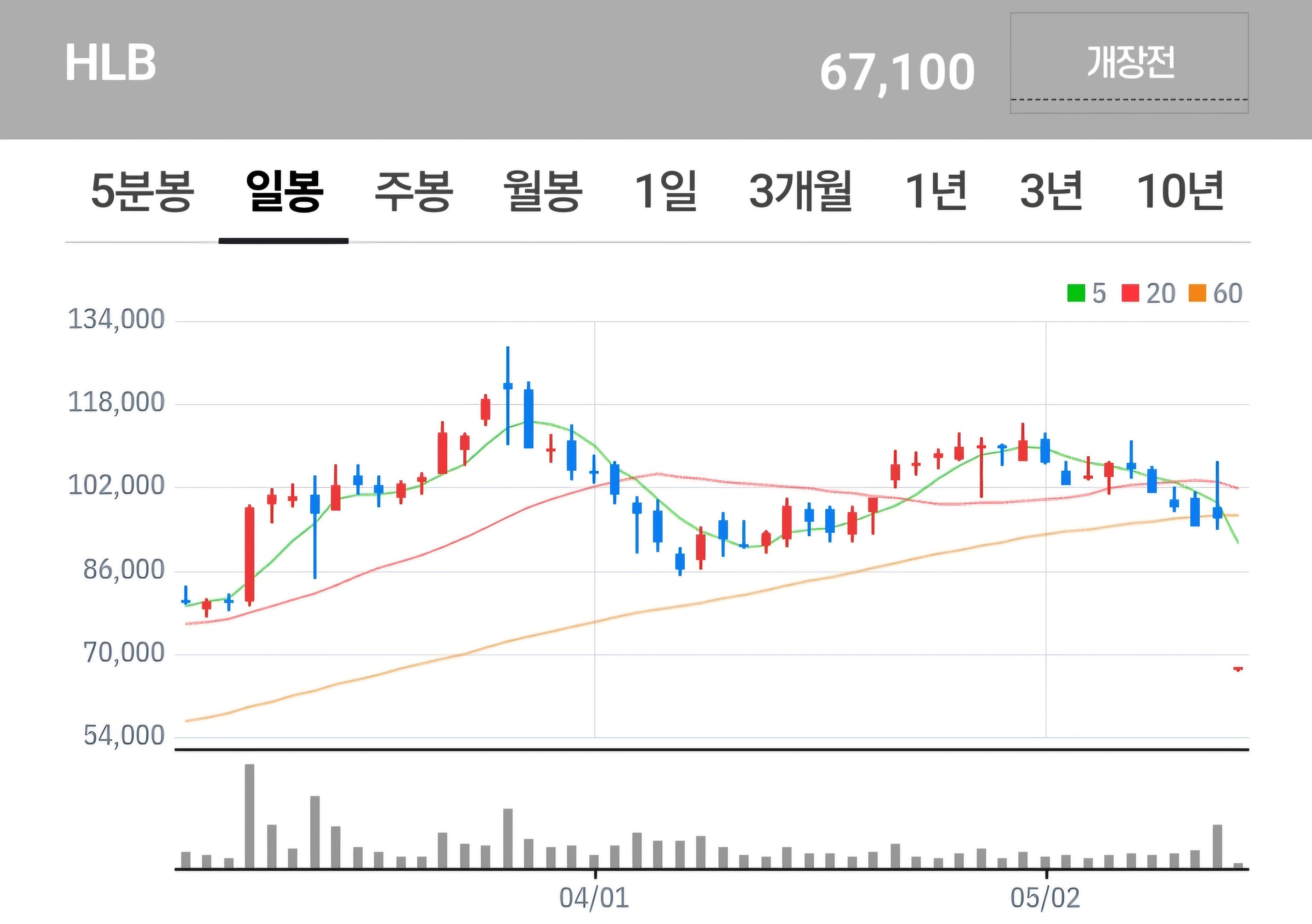
지금까지 HLB 하한가 쇼크, 리보세라닙 FDA 승인 거절에 대해서 알아보았습니다.
'경제를 배우자.' 카테고리의 다른 글
| 하나마이크론 급락, 유무상증자 발표 (하나머티리얼즈) (0) | 2024.05.20 |
|---|---|
| 그린플러스, ‘시서스 원료’ 식약처 승인 (1) | 2024.05.20 |
| HPSP 24년 1분기 실적 및 자사주 취득 공시 (1) | 2024.05.19 |
| 미국 4월 소비자물가지수(CPI) 둔화, 4월 소매판매 컨센 하회에 미증시 랠리 (1) | 2024.05.16 |
| 미국 4월 생산자 물가 지수(PPI) 컨센서스 상회 및 파월의장 발언 (0) | 2024.05.16 |




댓글